2. 多媒体与智能软件技术北京市重点实验室,北京 100124;
3. 北京人工智能研究院,北京 100124
2. Beijing Municipal Key Laboratory of Multimedia and Intelligent Software Technology, Beijing 100124, China;
3. Beijing Artificial Intelligence Institute, Beijing 100124, China
近期脑科学研究发现许多神经精神类疾病与脑功能连接的异常变化有关, 表明脑功能连接可作为神经精神类疾病诊断的一种有效的生物标记物[1-2]. 于是, 近年来面向神经精神类疾病诊断任务, 基于功能磁共振成像(functionalmagnetic resonance imaging, fMRI)技术的脑功能连接分类引起了研究人员的极大兴趣[3-5], 研究人员希望通过计算机辅助技术来提高神经精神类疾病诊断的准确性. 然而, 分类方法的准确性很大程度上依赖于所使用的脑功能连接判别特征, 因此, 如何从高维的脑功能连接数据中识别出脑功能连接判别特征成为了脑科学领域研究的一项重要课题.
目前, 脑功能连接判别特征的识别方法主要包括特征提取和特征选择两类方法. 其中, 特征提取方法通过某种线性变换将脑功能连接数据从高维特征空间映射到低维特征空间, 并把低维空间的特征作为判别特征. 例如, 文献[6]采用主成分分析方法(principal component analysis, PCA)提取鉴别性特征, 进而将中风患者分类到不同的治疗阶段. 文献[7]采用局部线性嵌入方法(locally linear embedding, LLE)获取低维特征, 并通过自组织功能磁共振聚类来区分精神分裂症患者和正常被测试者. 特征提取方法对脑功能连接特征形式进行了转换, 获得的判别特征不易理解, 不利于医生进行疾病诊断和给出神经学解释. 特征选择方法依据度量指标从高维的脑功能连接特征中挑选若干个度量值高的特征作为判别特征, 不会改变脑功能连接的原始特征形式. 例如, 文献[8]使用非模型打分方法(
粗糙集是一种处理不精确、不一致和不确定知识的数学工具, 它能够在不改变知识系统原有特征形式且充分考虑特征相关性的前提下发现关键的特征. 并且, 粗糙集理论经过多年的发展已经包含了处理各种数据类型的模型, 如处理连续型数据的邻域粗糙集[10], 处理噪声数据的决策粗糙集[11], 处理连续噪声数据的邻域决策粗糙集[12]等. 其中邻域决策粗糙集由于结合了邻域粗糙集处理连续型数据和决策粗糙集处理噪声数据的优势, 近年来逐渐获得了一些学者的关注. 文献[13]以减小边界区域、降低总体决策代价以及增大邻域半径为原则, 结合多目标优化的方法对邻域决策粗糙集中的邻域半径和概率阈值进行了求解; 文献[14]提出混合型信息系统下的邻域决策粗糙集模型, 并给出了该模型的增量式更新算法; 文献[15]将局部策略引入邻域决策粗糙集, 以识别异常数据, 并利用粒子群优化算法为模型提供最优的邻域粒度. 这些研究工作显示了邻域决策粗糙集在特征约简、增量学习以及异常数据检测等数据挖掘领域的优异性能.
鉴于脑功能连接是体现脑区之间功能关联程度的连续型数据, 且因各种主客观因素的影响含有许多噪声, 本文提出一种基于邻域决策粗糙集的脑功能连接生物标记物识别方法(identifying brain functional connectivity biomarkers based on neighborhood decision rough set, BNDRS). 具体来说, 本文根据邻域决策粗糙集的正域大小来衡量脑功能连接特征子集的分类能力, 采用添加-删除操作[16]搜索脑功能连接判别特征. 为了保证搜索效率, 本文首先利用哈希映射[17]和邻域关系的对称性[18]快速得到被试的邻域; 其次基于特征可分性度量[19]对脑功能连接特征进行分组来产生粗粒度特征搜索空间. 在ABIDE I和ADNI数据集上与多个方法的实验结果表明, 本文所提出方法能够高效地获得分类能力更强的脑功能连接判别特征, 有望为神经精神类疾病的诊断和治疗提供更加准确的生物标记物.
本文剩余部分的组织结构如下: 第1节介绍邻域决策粗糙集的基本知识; 第2节详细阐述本文所提出的基于邻域决策粗糙集的脑功能连接生物标记物识别方法; 第3节通过实验验证所提出方法的有效性; 第4节对本文工作进行总结并指出下一步的研究方向.
1 邻域决策粗糙集在邻域决策粗糙集中, 决策表由一个四元组
| $ \begin{align} \delta_{B}(x)=\{x_{i}|x_{i}\in U, d_{B}(x, x_{i})\leqslant\delta\}. \end{align} $ | (1) |
其中:
| $ \begin{align} d_{B}(x, x_{i})=\Big( \sum\limits_{j=1}^{m}|I_{a_{j}}(x)-I_{a_{j}}(x_{i})|^2\Big)^{\frac{1}{2}}. \end{align} $ | (2) |
| $ \begin{align} P(X|\delta_{B}(x))=\frac{|\delta_{B}(x) \bigcap X|}{|\delta_{B}(x)|}, \end{align} $ | (3) |
其中
邻域决策粗糙集中任意样本集
1) 若
2) 若
3) 若
其中: 概率阈值
| $ \begin{align} \alpha=\frac{\lambda_{\rm PN}-\lambda_{\rm BN}}{(\lambda_{\rm PN}-\lambda_{\rm BN}) + (\lambda_{\rm BP}-\lambda_{\rm PP})}, \end{align} $ | (4) |
| $ \begin{align} \beta=\frac{\lambda_{\rm BN}-\lambda_{\rm NN}}{(\lambda_{\rm BN}-\lambda_{\rm NN}) + (\lambda_{\rm NP}-\lambda_{\rm BP})}. \end{align} $ | (5) |
决策代价满足以下条件[11]:
| $ \begin{align} \frac{\lambda_{\rm NP}-\lambda_{\rm BP}}{\lambda_{\rm BN}-\lambda_{\rm NN}}>\frac{\lambda_{\rm BP}-\lambda_{\rm PP}}{\lambda_{\rm PN}-\lambda_{\rm BN}}. \end{align} $ | (6) |
若用
| $ \begin{align} &{\rm POS}_{B}(\pi_{D})= \bigcup\limits_{1\leqslant i\leqslant m}{\rm POS}_{B}(D_{i}), \end{align} $ | (7) |
| $ \begin{align} &{\rm BND}_{B}(\pi_{D})= \bigcup\limits_{1\leqslant i\leqslant m}{\rm BND}_{B}(D_{i}), \end{align} $ | (8) |
| $ \begin{align} &{\rm NEG}_{B}(\pi_{D})=U-{\rm POS}_{B}(\pi_{D}) \bigcup {\rm BND}_{B}(\pi_{D}). \end{align} $ | (9) |
邻域决策粗糙集可基于正域衡量相应特征子集的判别能力, 并利用添加-删除操作来寻找分类能力强的特征子集.令
| $ \begin{align} {\rm SIG}(c)=|{\rm POS}_{R\bigcup \{c\}}(\pi_{D})|-|{\rm POS}_{R}(\pi_{D})|. \end{align} $ | (10) |
从当前特征子集
| $ \begin{align} {\rm SIG}(r)=|{\rm POS}_{R}(\pi_{D})|-|{\rm POS}_{R-\{r\}}(\pi_{D})|. \end{align} $ | (11) |
上述特征约简过程的时间复杂度为
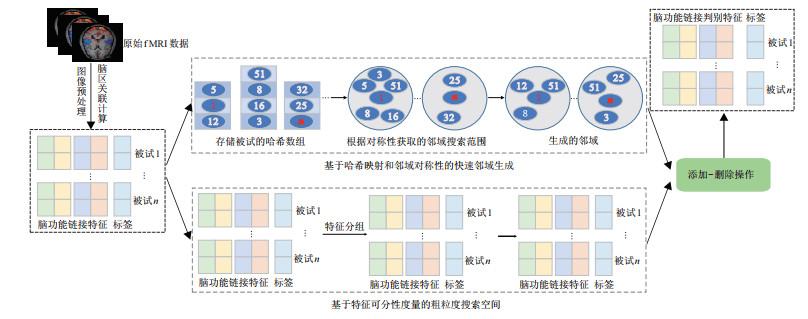
本节将详细介绍本文所提出的基于邻域决策粗糙集的脑功能连接生物标记物识别方法(BNDRS). BNDRS根据邻域决策粗糙集正域的大小衡量相应脑功能连接特征子集的分类能力, 采用添加-删除操作搜索脑功能连接判别特征, 并通过快速生成邻域和缩小特征搜索空间来保证其时间性能. BNDRS的流程如图 1所示, 接下来将对BNDRS包含的主要步骤和机制进行详细介绍.
|
图 1 本文所提BNDRS方法的示意图 |
为了减小生成被试邻域的时间复杂度, BNDRS对被试进行哈希映射, 将每个被试映射到以数组作为存储结构的哈希表中. 对于脑功能连接特征子集
| $ \begin{align} H_{B}(x)=\Big\lceil\frac{d_{B}(x, x_{0})}{\delta}\Big\rceil. \end{align} $ | (12) |
其中:
| $ \begin{align} A_{k}=\{x_{i}|x_{i}\in U, k=H_{B}(x_{i})\}. \end{align} $ | (13) |
基于上面的哈希映射, 可以证明任意被试的邻域至多存在于该被试所在的数组以及与该被试相邻的数组. 下面给出上述结论的证明过程.
证明 对于任意被试
| $ \begin{align} k\delta\geqslant d_{B}(x, x_{0})>(k-1)\delta. \end{align} $ | (14) |
对于任意被试
| $ \begin{align} (k+2)\delta\geqslant d_{B}(x_{i}, x_{0})>(k+1)\delta. \end{align} $ | (15) |
结合式(11)和(12)可得
| $ \begin{align} d_{B}(x_{i}, x_{0})-d_{B}(x, x_{0})>\delta. \end{align} $ | (16) |
若被试
| $ \begin{align} d_{B}(x, x_{i})>d_{B}(x_{i}, x_{0})-d_{B}(x, x_{0})>\delta; \end{align} $ | (17) |
若被试
| $ \begin{align} d_{B}(x, x_{i})\geqslant d_{B}(x_{i}, x_{0})-d_{B}(x, x_{0})>\delta. \end{align} $ | (18) |
由式(14)和(15)可知, 对于任意被试
邻域关系具有对称性, 即若被试
综上, 将被试映射到哈希数组后, 结合邻域关系的对称性, 对于数组
特征可分性度量是一种根据特征在同类样本的相似程度和不同类样本的差异程度来衡量其分类能力的度量指标, 计算公式如下:
| $ \begin{align} {\rm ASM}(c)=\frac{|\mu_{+}(c)-\mu_{-}(c)|}{\sigma_{+}(c)+\sigma_{-}(c)}. \end{align} $ | (19) |
其中:
由式(16)可知, 特征可分性度量值越大, 表明相应脑功能连接特征对不同类别被试的区分度越大, 对相同类别被试的区分度越小, 可见特征可分性度量可以反映脑功能连接特征的分类能力. 若将特征可分性度量值较大的若干特征同时加入到当前脑功能连接特征子集中, 则有望快速增加该特征子集的分类能力.然而, 具有较大特征可分性度量值的若干脑功能连接特征有可能与当前脑功能连接特征子集中已有的特征存在冗余. 因此, 在对当前脑功能连接特征子集进行添加操作时, 需要计算各个特征组合的重要度, 然后再将重要度最大的特征组合中的特征添加至当前脑功能连接特征子集. 特征组合重要度的计算公式如下:
| $ \begin{align} {\rm SIG}(f)={\rm POS}_{|R\bigcup f|}(\pi_{D})-{\rm POS}_{R}(\pi_{D}). \end{align} $ | (20) |
其中:
根据上面的描述, 基于特征可分性度量的脑功能连接特征分组策略实现的具体步骤为: 首先计算每个脑功能连接特征的特征可分性度量值; 然后根据特征可分性度量值对脑功能连接特征进行降序排序; 最后设定划分步长
基于前面的描述, 给出基于邻域决策粗糙集的脑功能连接生物标记物识别算法的伪代码如下.
算法1 基于邻域决策粗糙集的脑功能连接生物标记物识别算法.
step 1: 输入被试的脑功能连接特征集
step 2: 初始化脑功能连接判别特征集
step 3: 基于哈希映射和邻域对称性生成被试关于
step 4: 基于特征可分性度量对
step 5: 结合基于哈希映射和邻域对称性的快速邻域生成策略计算每一个特征组合的重要度, 并将重要度最大的特征组合中的脑功能连接特征添加至
step 6: 删除
step 7: 输出
算法1的时间复杂度取决于step 5, 设哈希数组的数量为
本节通过实验来验证所提出方法的有效性, 实验的运行环境为Windows 10操作系统, 处理器为Inter(R) Core(TM) i5-6500 CPU 3.20G Hz, RAM为12 G. 算法利用Matlab R2018b运行工具编写的Matlab代码完成.
3.1 实验数据及评价标准 3.1.1 实验数据本文实验所使用的数据集来自: 自闭症脑成像数据交换联盟发布的ABIDE I数据集和阿尔茨海默症神经影像学联盟发布的ADNI数据集. 其中ABIDE I数据集包含569名正常被试和525名自闭症患者, ADNI数据集包括66名正常被试和53名阿尔茨海默症患者.
从以上数据集中获取的原始fMRI数据首先需要经过层间时间校正、头动校正等一系列图像预处理操作, 然后采用AAL模板进行脑区的划分, 并使用皮尔森相关系数计算不同脑区之间相互关联的程度, 得到脑功能连接矩阵, 最后将脑功能连接矩阵的上三角或下三角展开, 即可获得脑功能连接数据. 由于神经精神类疾病主要由大脑皮层脑区之间功能连接的障碍引起, 本文只选取位于大脑皮层的90个脑区进行脑区功能关联的计算, 最终获取的脑功能连接特征的维数为4 005.
3.1.2 评价标准本文主要从以下3个方面评价脑功能连接生物标记物识别方法的性能: 获得的脑功能连接判别特征的数量Nu; 时间消耗
| $ \begin{align} &{\rm Acc}=\frac{{\rm TP}+{\rm TN}}{{\rm TP}+{\rm FP}+{\rm TN}+{\rm FN}}, \end{align} $ | (21) |
| $ \begin{align} &{\rm Pr}=\frac{{\rm TP}}{{\rm TP}+{\rm FP}}, \end{align} $ | (22) |
| $ \begin{align} &{\rm Re}=\frac{{\rm TP}}{{\rm TP}+{\rm FN}}, \end{align} $ | (23) |
| $ \begin{align} &{\rm Fm}=\frac{2\times {\rm Pr}\times {\rm Re}}{{\rm Pr}+{\rm re}}. \end{align} $ | (24) |
其中: TP是将患者被试预测为患者的数目, TN是将正常被试预测为正常人的数目, FP是将正常被试预测为患者的数目, FN是将患者被试预测为正常人的数目.
3.2 参数设置本文测试了BNDRS在不同参数取值下所得脑功能连接判别特征的分类能力, 在ABIDE I和ADNI数据集上, 测试的概率阈值的范围为: 0.5、0.6、0.7、0.8、0.9, 测试的邻域半径的范围为: 0.4、0.5、0.6、0.7、0.8.在ABIDE I数据集上测试的划分步长的范围为: 11、15、19、23、27, 在ADNI数据集上测试的划分步长的范围为: 5、10、15、20、25.
测试结果显示在ABIDE I数据集和ADNI数据集上, 对于不同的参数取值, BNDRS所得脑功能连接判别特征的分类能力整体上较平稳, 并且, 当邻域半径取0.4、概率阈值取0.6、划分步长取19时, BNDRS在ABIDE I数据集上获得了分类能力最强的脑功能连接判别特征. 当邻域半径取0.8、概率阈值取0.9、划分步长取5时, BNDRS在ADNI数据集上获得了分类能力最强的脑功能连接判别特征. 因此, 为了获得分类能力最强的脑功能连接特征, 本文在ABIDE I数据集上将邻域半径设置为0.4、概率阈值设置为0.6、划分步长设置为19. 在ADNI数据集上将邻域半径设置为0.8、概率阈值设置为0.9、划分步长设置为5.
3.3 策略验证本节实验验证BNDRS中基于哈希映射和邻域对称性的快速邻域生成策略以及基于特征可分性度量的脑功能连接特征分组策略的效果. 实验设计了2个BNDRS的变异算法: BNDRS-F和BNDRS-H. 其中, BNDRS-F在BNDRS基础上去除了基于哈希映射和邻域对称性的快速邻域生成策略, BNDRS-H在BNDRS基础上去掉了基于特征可分性度量的脑功能连接特征分组策略. 实验使用的数据集是ABIDE I数据集, 实验结果如表 1所示.
| 表 1 BNDRS与两个变异算法的比较 |
对比BNDRS和BNDRS-F可以看出, 两者在Acc、Pr、Re、Fm、Nu五个指标上均相同, 说明基于哈希映射和邻域对称性的快速邻域生成策略可以正确获取被试的邻域, 不会影响算法的准确性. 同时还可从表 1看出, BNDRS的耗时小于BNDRS-F. 实验结果表明, 基于哈希映射和邻域对称性的快速邻域生成策略可以在不影响算法所得脑功能连接判别特征分类能力的前提下, 提高算法的时间性能.
对比BNDRS和BNDRS-H可以看出, 与BNDRS-H相比, BNDRS在Acc、Pr、Re、Fm四个指标上均大于BNDRS-H. 并且BNDRS的耗时远小于BNDRS-H的耗时. 实验结果表明, 基于特征可分性度量的脑功能连接特征分组策略不仅能大幅度提高邻域决策粗糙集的时间性能, 还可以提高邻域决策粗糙集所获得的脑功能连接判别特征的分类能力.
3.4 特征约简能力验证本节对BNDRS的特征约简能力进行验证, 实验设计了1个变异算法: BNRS, 该算法将BNDRS中的概率阈值设为1, 不具备噪声处理能力. 实验使用ABIDE I数据集, 实验结果如表 2所示. 表 2中C代表未约简的原脑功能连接特征, BNDRS_C代表使用BNDRS得到的脑功能连接判别特征, BNRS_C代表使用BNRS得到的脑功能连接判别特征.
| 表 2 不同脑功能连接特征分类能力和数量的比较 |
由表 2可以看出, 与第1行未约简的原脑功能连接特征对比, BNDRS所得脑功能连接判别特征的数量大幅减少, 并且BNDRS所得脑功能连接判别特征在指标Acc、Pr、Re、Fm上都较高. 该实验结果说明BNDRS有能力删除大量的冗余脑功能连接特征, 获得分类能力更强的脑功能连接判别特征. 与第3行不具备噪声处理能力的BNRS相比, BNDRS所得脑功能连接判别特征在指标Acc、Pr、Re、Fm上也较高. 该实验结果说明BNDRS在约简高维脑功能连接数据的过程中, 可对噪声数据进行较好地处理. 以上实验结果验证了BNDRS具有较强的特征约简能力.
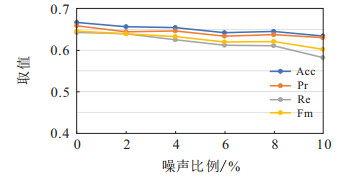
3.5 鲁棒性验证本节在ABIDE I数据集上验证BNDRS的鲁棒性. 首先随机挑选ABIDE I数据集上5种不同比例(2 %、4 %、6 %、8 %、10 %)的被试, 然后为这些选出的被试添加高斯噪声, 最后在5个带有不同比例噪声的ABIDE I数据集上测试BNDRS所得到的脑功能连接判别特征的分类能力. 实验结果如图 2所示.
|
图 2 不同噪声比例下的实验结果 |
由图 2可以看出, 当噪声比例为2 %、4 %、6 %、8 %时, 与没有添加噪声的数据(噪声比例为0 %)相比, 指标Acc、Pr、Re、Fm的值波动较小, 表明BNDRS在上述不同比例的噪声下仍能获得分类能力比较强的脑功能连接判别特征. 当噪声比例达到10 %时, 与没有添加噪声的数据(噪声比例取0 %)对比, 指标Pr、Re、Fm的值下降相对较多, 但指标Acc依然保持在一个不错的水平. 上述实验结果表明, BNDRS在10 %以内的噪声比例下有不错的抗噪声干扰能力, 具有较强的鲁棒性.
3.6 脑功能连接生物标记物识别方法对比本节将所提出的BNDRS与PCA[6]、LLE[7]、
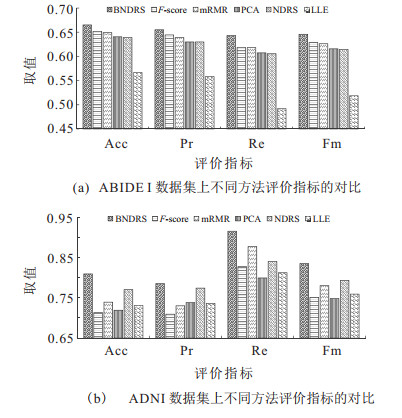
图 3展示了不同方法所得脑功能连接判别特征的分类指标值. 由图 3可以看出, 对于实验使用的两个数据集, BNDRS在Acc、Pr、Re、Fm四个指标上的值均大于对比方法, 且在ADNI数据集上, BNDRS所得脑功能连接判别特征分类能力的优势尤为显著. 该实验结果表明, 与对比方法相比, BNDRS所得脑功能连接判别特征具有更强的分类能力.
|
图 3 各数据集上不同方法评价指标的对比 |
不同方法的约简耗时及所得脑功能连接判别特征数量的对比如表 3所示. 由表 3可以看出, 在实验使用的所有数据集上, BNDRS获得脑功能连接判别特征的时间消耗均远小于NDRS. 此外, 在ABIDE I数据集上, BNDRS获得脑功能连接判别特征的时间消耗小于mRMR.
| 表 3 不同方法时间性能及所得脑功能连接判别特征数量的比较 |
由表 3还可以看出, BNDRS获得的脑功能连接判别特征的数量在ABIDE I和ADNI数据集上均仅多于NDRS, 这是因为BNDRS具有强大的特征约简能力, 可去除大量的冗余脑功能连接特征.
3.6.3 生物标记物对比本文对比的所有方法中, PCA和LLE对脑功能连接数据的特征形式进行了转换, 无法根据约简获得的特征定位到相关联的脑区, 所以本节只对BNDRS、mRMR、
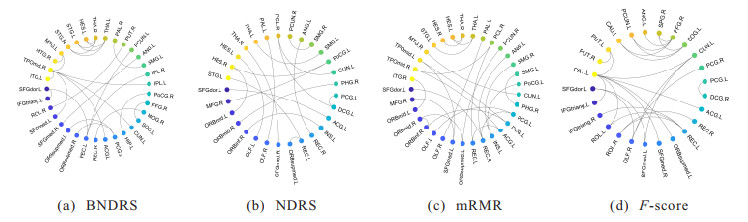
图 4展示了4种方法在ABIDE I数据集上得到的脑功能连接判别特征所对应的脑区连接情况. 由图 4可以看出, 在ABIDE I数据集上, BNDRS得到的脑功能连接判别特征涉及上述与自闭症相关的所有脑区, 而NDRS和mRMR得到的脑功能连接判别特征不涉及与自闭症相关的梭状回(FFG.L, FFG.R),
|
图 4 ABIDE I数据集上不同方法对应生物标记物的对比 |
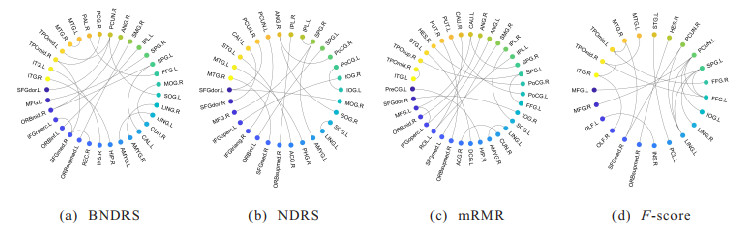
图 5展示了4种方法在ADNI数据集上得到的脑功能连接判别特征所对应的脑区连接情况. 可以看出, 在ADNI数据集上, BNDRS涉及与阿尔茨海默症相关的后扣带回(PCG.R)、楔前叶(PCUN.R)、颞中回(MTG.L, MTG.R)、颞下回(ITG.L, ITG.R); NDRS涉及与阿尔茨海默症相关的颞中回(MTG.L, MTG.R)、楔前叶(PCUN.L, PCUN.R); mRMR涉及与阿尔茨海默症相关的颞下回(ITG.L)、中央前回(PreCG.L);
|
图 5 ADNI数据集上不同方法对应生物标记物的对比 |
从以上实验结果可看出, 在ABIDE I和ADNI数据集上, BNDRS分别定位到了最多数量的与自闭症和阿尔茨海默症相关的脑区. 因此, BNDRS有望为神经精神类疾病的诊断提供更准确的脑功能连接生物标记物.
4 结论本文提出了一种新的面向神经精神类疾病的脑功能连接生物标记物识别方法. 该方法针对脑功能连接数据的连续性和高噪声的特点, 利用能有效处理连续和高噪声数据的邻域决策粗糙集来识别与神经精神类疾病高度相关的脑功能连接判别特征; 针对脑功能连接数据的高维特点, 该方法通过快速生成邻域和缩小特征搜索空间来提高邻域决策粗糙集识别脑功能连接判别特征的效率. 实验结果表明, 该方法可以高效地获得分类能力更强的脑功能连接判别特征, 更加准确定位与脑疾病相关的脑区, 进而为神经精神类疾病的诊断提供更准确的生物标记物.
下一步的工作将研究融合不同邻域半径下的粒度信息, 探索面向脑功能连接数据的邻域决策粗糙集多粒度特征约简方法, 进一步提高获得的脑功能连接生物标记物的准确性.
| [1] |
Lynall M E, Bassett D S, Kerwin R, et al. Functional connectivity and brain networks in schizophrenia[J]. The Journal of Neuroscience, 2010, 30(28): 9477-9487. DOI:10.1523/JNEUROSCI.0333-10.2010 |
| [2] |
Zhang J R, Wang J H, Wu Q Z, et al. Disrupted brain connectivity networks in drug-naive, first-episode major depressive disorder[J]. Biological Psychiatry, 2011, 70(4): 334-342. DOI:10.1016/j.biopsych.2011.05.018 |
| [3] |
Rosa M J, Portugal L, Hahn T, et al. Sparse network-based models for patient classification using fMRI[J]. NeuroImage, 2015, 105: 493-506. DOI:10.1016/j.neuroimage.2014.11.021 |
| [4] |
Challis E, Hurley P, Serra L, et al. Gaussian process classification of Alzheimer's disease and mild cognitive impairment from resting-state fMRI[J]. NeuroImage, 2015, 112: 232-243. DOI:10.1016/j.neuroimage.2015.02.037 |
| [5] |
Rashid B, Arbabshirani M R, Damaraju E, et al. Classification of schizophrenia and bipolar patients using static and dynamic resting-state fMRI brain connectivity[J]. NeuroImage, 2016, 134: 645-657. DOI:10.1016/j.neuroimage.2016.04.051 |
| [6] |
Mohanty R, Sinha A M, Remsik A B, et al. Machine learning classification to identify the stage of brain-computer interface therapy for stroke rehabilitation using functional connectivity[J]. Frontiers in Neuroscience, 2018, 12: 353-366. DOI:10.3389/fnins.2018.00353 |
| [7] |
Shen H, Wang L B, Liu Y D, et al. Discriminative analysis of resting-state functional connectivity patterns of schizophrenia using low dimensional embedding of fMRI[J]. NeuroImage, 2010, 49(4): 3110-3121. DOI:10.1016/j.neuroimage.2009.11.011 |
| [8] |
Kong Y Z, Gao J L, Xu Y P, et al. Classification of autism spectrum disorder by combining brain connectivity and deep neural network classifier[J]. Neurocomputing, 2019, 324: 63-68. DOI:10.1016/j.neucom.2018.04.080 |
| [9] |
Hamdi S M, Aydin B, Filali Boubrahimi S, et al. Biomarker detection from fMRI-based complete functional connectivity networks[C]. The 1st International Conference on Artificial Intelligence and Knowledge Engineering. Laguna Hills, 2018: 17-24.
|
| [10] |
Hu Q H, Yu D R, Liu J F, et al. Neighborhood rough set based heterogeneous feature subset selection[J]. Information Sciences, 2008, 178(18): 3577-3594. DOI:10.1016/j.ins.2008.05.024 |
| [11] |
Yao Y Y, Zhao Y. Attribute reduction in decision-theoretic rough set models[J]. Information Sciences, 2008, 178(17): 3356-3373. DOI:10.1016/j.ins.2008.05.010 |
| [12] |
Li W W, Huang Z Q, Jia X Y, et al. Neighborhood based decision-theoretic rough set models[J]. International Journal of Approximate Reasoning, 2016, 69: 1-17. DOI:10.1016/j.ijar.2015.11.005 |
| [13] |
Pan R L, Wang X M, Yi C S, et al. Multi-objective optimization method for thresholds learning and neighborhood computing in a neighborhood based decision-theoretic rough set model[J]. Neurocomputing, 2017, 266: 619-630. DOI:10.1016/j.neucom.2017.05.068 |
| [14] |
苑红星, 卓雪雪, 竺德, 等. 基于矩阵的混合型邻域决策粗糙集增量式更新算法[J]. 控制与决策, 2022, 37(6): 1621-1631. (Yuan H X, Zhuo X X, Zhu D, et al. Incremental updating algorithms of neighborhood decision-theoretic rough set model for hybrid data based on matrix[J]. Control and Decision, 2022, 37(6): 1621-1631. DOI:10.13195/j.kzyjc.2020.1371) |
| [15] |
孙颖, 蔡天使, 张毅, 等. 基于合理粒度的局部邻域决策粗糙计算方法[J]. 南京大学学报: 自然科学, 2021, 57(2): 262-271. (Sun Y, Cai T S, Zhang Y, et al. Justifiable granularity based local neighborhood decision-theoretic rough set approach[J]. Journal of Nanjing University: Natural Science, 2021, 57(2): 262-271.) |
| [16] |
Yao Y Y, Zhao Y, Wang J. On reduct construction algorithms[C]. Proceedings of the 1st International Conference on Rough Sets and Knowledge Technology. Chong qing, 2006: 239-304.
|
| [17] |
Liu Y, Huang W L, Jiang Y L, et al. Quick attribute reduct algorithm for neighborhood rough set model[J]. Information Sciences, 2014, 271: 65-81. DOI:10.1016/j.ins.2014.02.093 |
| [18] |
胡清华, 于达仁, 谢宗霞. 基于邻域粒化和粗糙逼近的数值属性约简[J]. 软件学报, 2008, 19(3): 640-649. (Hu Q H, Yu D R, Xie Z X. Numerical attribute reduction based on neighborhood granulation and rough approximation[J]. Journal of Software, 2008, 19(3): 640-649.) |
| [19] |
Ma Y Y, Luo X Y, Li X L, et al. Selection of rich model steganalysis features based on decision rough set α-positive region reduction[J]. IEEE Transactions on Circuits and Systems for Video Technology, 2019, 29(2): 336-350. DOI:10.1109/TCSVT.2018.2799243 |
| [20] |
Li H L, Parikh N A, He L L. A novel transfer learning approach to enhance deep neural network classification of brain functional connectomes[J]. Frontiers in Neuroscience, 2018, 12: 491. DOI:10.3389/fnins.2018.00491 |
| [21] |
Heinsfeld A S, Franco A R, Craddock R C, et al. Identification of autism spectrum disorder using deep learning and the ABIDE dataset[J]. NeuroImage: Clinical, 2018, 17: 16-23. DOI:10.1016/j.nicl.2017.08.017 |
| [22] |
Lynch C J, Uddin L Q, Supekar K, et al. Default mode network in childhood autism: Posteromedial cortex heterogeneity and relationship with social deficits[J]. Biological Psychiatry, 2013, 74(3): 212-219. DOI:10.1016/j.biopsych.2012.12.013 |
| [23] |
Uddin L Q, Supekar K, Lynch C J, et al. Salience network-based classification and prediction of symptom severity in children with autism[J]. JAMA Psychiatry, 2013, 70(8): 869-879. DOI:10.1001/jamapsychiatry.2013.104 |
| [24] |
He Y, Wang L, Zang Y F, et al. Regional coherence changes in the early stages of Alzheimer's disease: A combined structural and resting-state functional MRI study[J]. NeuroImage, 2007, 35(2): 488-500. DOI:10.1016/j.neuroimage.2006.11.042 |
| [25] |
Buckner R L, Sepulcre J, Talukdar T, et al. Cortical hubs revealed by intrinsic functional connectivity: Mapping, assessment of stability, and relation to Alzheimer's disease[J]. The Journal of Neuroscience, 2009, 29(6): 1860-1873. DOI:10.1523/JNEUROSCI.5062-08.2009 |
| [26] |
Daianu M, Jahanshad N, Nir T M, et al. Rich club analysis in the Alzheimer's disease connectome reveals a relatively undisturbed structural core network[J]. Human Brain Mapping, 2015, 36(8): 3087-3103. DOI:10.1002/hbm.22830 |
 2023, Vol. 38
2023, Vol. 38
